4,3 millions
séances de radiothérapie sont effectuées en 2021 en faveur de 214 000 patients.
Arme majeure de lutte contre le cancer, la radiothérapie n’est pas dénuée d’effets secondaires pour les patients. Quel est l’avis des experts sur les nouvelles techniques utilisées en radiothérapie ? Quelles recherches sont menées sur les effets secondaires après traitement ? Les scientifiques de l’IRSN veillent à réduire les risques à chaque étape des traitements.

Utiliser des rayonnements ionisants pour attaquer une tumeur, voilà le principe de la radiothérapie (voir infographie "Radiothérapie : bienfaits et écueils"). « Plus de 50 % de patients atteints de cancer reçoivent une radiothérapie au cours du traitement de leur maladie. C’est le pilier principal de la lutte contre le cancer », rappelle Philippe Maingon, oncologue-radiothérapeute à l’hôpital de la Pitié-Salpêtrière à Paris. Et les techniques évoluent en permanence.
À Fontenay-aux-Roses (Hauts-de-Seine), les spécialistes de l’IRSN expertisent des traitements et des appareils innovants, contribuant à leur utilisation correcte. Pour mieux protéger les patients, leurs recherches englobent les effets secondaires de l’imagerie médicale afin de limiter les risques de cancers radio-induits. Repères fait le point.
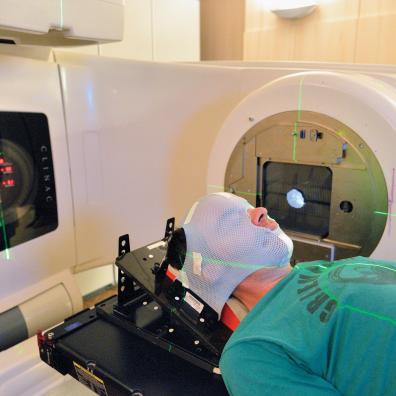
En 2017, l’Autorité de sûreté nucléaire demande à l’Unité d’expertise en radioprotection médicale (UEM) d’étudier la mise en œuvre des IRM-Linac. Ces accélérateurs linéaires sont couplés à l’imagerie par résonance magnétique (IRM). En France, l’Institut Paoli-Calmettes à Marseille (Bouches du -Rhône) est le premier à l’utiliser. Le champ magnétique dû à l’IRM pose question. « Quel est l’impact sur la prise en charge des patients et quel est le contrôle qualité à réaliser ? », Aurélie Isambert, spécialiste en radioprotection médicale, résume les inquiétudes des experts.
L’IRSN forme un groupe de travail avec la Société française de physique médicale (SFPM). En 2017 et 2018, ils auditionnent les fabricants, examinent la littérature et visitent des hôpitaux qui en sont équipés aux Pays-Bas. « Un travail en complémentarité », relate Vincent Marchesi, vice-président de la SFPM. Cette expertise – avis 2018-00232 – compte plusieurs recommandations : ajuster le réglage des accélérateurs à proximité, s’assurer que les physiciens et radiothérapeutes impliqués possèdent des compétences solides en IRM, etc.
L’unité s’auto-saisit d’autres sujets. Exemple en 2022 : la radiothérapie Flash. En délivrant la dose en quelques millisecondes au lieu de quelques minutes, cette technique diminuerait les effets secondaires aux tissus sains pour un contrôle équivalent de la tumeur. « Nous suivons des avancées relatives à cette technique pour être prêts le jour où notre avis sera requis », indique l’experte.
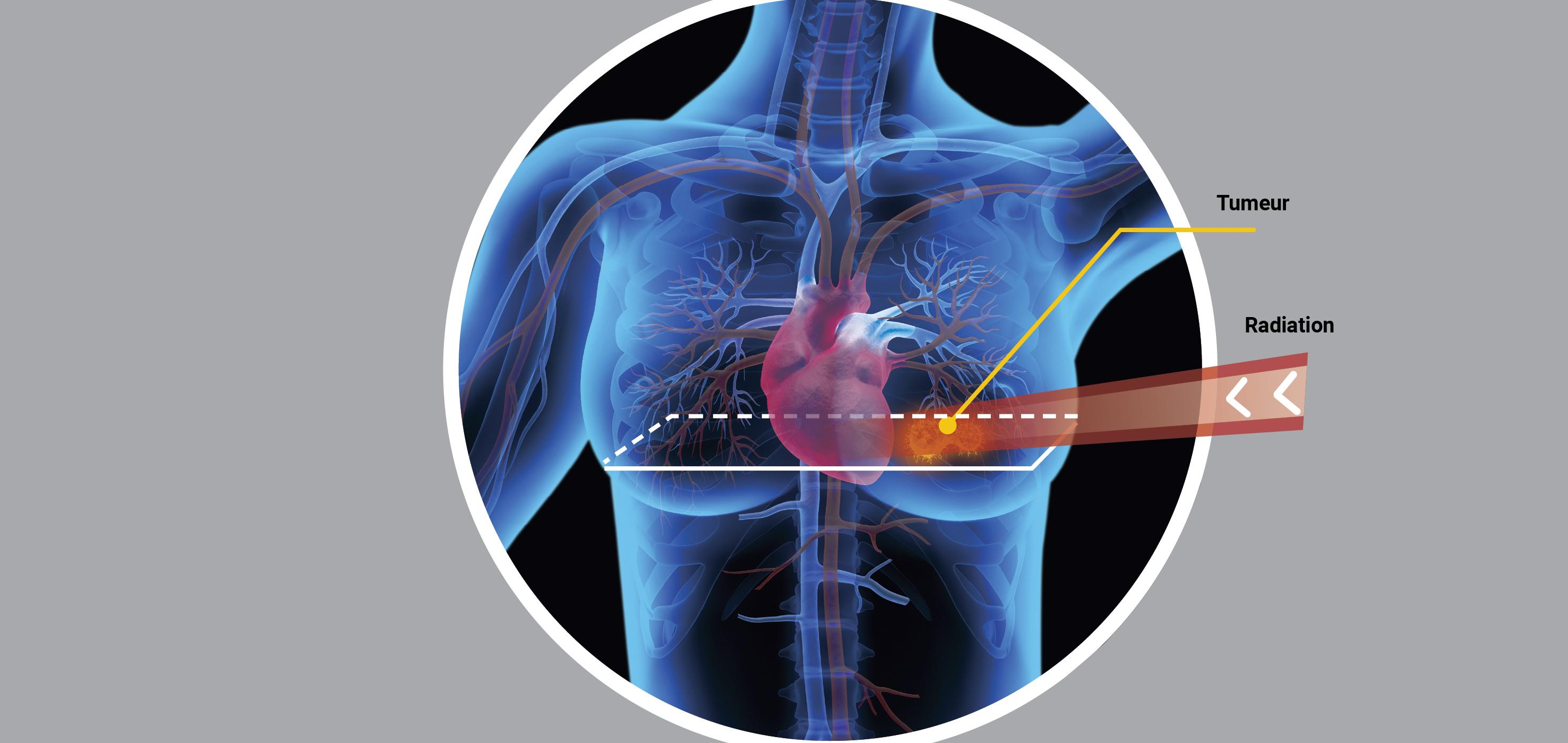
Minimiser les effets indésirables des traitements sur les tissus sains est une préoccupation de la radiothérapie. Elle est au coeur du plan de traitement établi en amont par les physiciens médicaux. « Il vise à garantir une distribution de dose au plus près de la tumeur », précise Philippe Maingon. Problème: « Les modèles de calcul servant à l’établir ne prennent pas en compte l’ensemble de l’irradiation », pointe Christelle Huet, chercheuse au Laboratoire de dosimétrie des rayonnements ionisants (LDRI), à Fontenay-aux-Roses. Ils intègrent le faisceau de rayonnement, mais pas celui diffusé, ni les fuites au niveau de la tête de l’appareil. Or cette irradiation non contrôlée pourrait augmenter le risque de cancers radio-induits à l’âge adulte chez des enfants traités par radiothérapie.
Pour mieux l’estimer et comparer différentes techniques de radiothérapie pédiatrique, la doctorante en radiophysique médicale au LDRI Julie Colnot conçoit en 2019 un outil expérimental : un fantôme 3D équipé de films noircissant en fonction de l’irradiation. « Il permet d’évaluer la dose reçue par les tissus sains », détaille Christelle Huet. Julie Colnot développe aussi un outil évaluant les doses aux tissus sains délivrées par le Cyberknife, un appareil de radiothérapie administrant des doses élevées avec une précision inférieure au millimètre. Il simule les faisceaux depuis leur production, jusqu’à leur absorption par les tissus.
L’évaluation des doses aux tissus sains proches de la tumeur est essentielle pour caractériser les effets secondaires pouvant se manifester des années après la radiothérapie. Le cœur est ainsi à risque dans la radiothérapie du cancer du sein. À partir de 2015, l’IRSN conçoit et pilote l’étude Baccarat1. Elle suit pendant deux ans 118 femmes traitées pour ce cancer à la Clinique Pasteur à Toulouse (Haute-Garonne). Baccarat évalue la survenue d’anomalies cardiaques asymptomatiques, dites infracliniques.
Pour élargir sa portée, la chercheuse collabore en 2017 à l’étude européenne multicentrique Medirad Early-Heart. Espagne, Portugal, Pays-Bas, Allemagne : quatre autres pays sont impliqués, soit 250 patientes en tout. Les premiers résultats révèlent une dysfonction de contraction du myocarde en lien avec l’exposition de cœur et du ventricule gauche. « Ils plaident pour un suivi renforcé de la fonction cardiaque après thérapie et une dosimétrie du cœur entier et de ses sous-structures : ventricule gauche... Cela pourrait améliorer la prévention », conclut l’épidémiologiste Sophie Jacob.
Pour élargir les connaissances, les épidémiologistes initient deux études. Radio-Aide2 porte sur la toxicité neurologique potentielle de la radiothérapie du cerveau : 250 patients de la cohorte EpibrainRad3 traités pour un gliome – tumeur du cerveau ou de la moelle épinière – sont suivis. Start4, évalue le risqué de complications salivaires chez les patients atteints d’un cancer de la thyroïde traités à l’iode radioactif. Les premiers résultats sont attendus respectivement en 2025 et 2023.
Comprendre les mécanismes biologiques menant aux lésions radio-induites est crucial. La radiothérapie stéréotaxique, prometteuse notamment pour les cancers du poumon, délivre une dose plus forte qu’un traitement conventionnel sur une zone de quelques millimètres. Par exemple, 60 grays sont délivrés en trois séances au lieu de trente séances en fraction de 2 grays. « Il y a peu de données sur la réponse de petits volumes de tissus sains irradiés à forte dose par fraction », observe Fabien Milliat, spécialiste en radiobiologie.
Pour analyser les effets de ce type d’irradiation, son équipe utilise depuis 2015 un dispositif préclinique, qui reproduit chez la souris des lésions proches de celles des humains. Elle s’intéresse à la sénescence* – le vieillissement accéléré des cellules – affectant ces lésions et les processus menant à des dysfonctions de type fibrose, dues aux durcissements d’organes. L’enjeu : trouver des cibles thérapeutiques visant la senescence radio-induite ou de la réponse immunitaire, pour in fine limiter les effets secondaires.
* Soysouvanh F et al. (2020) Int J Radiat Oncol Biol Phys 106, 1017-27.
1. Breast Cancer and Cardiotoxicity induced by Radiotherapy, www.irsn.fr/etude-baccarat
2. Radiation-induced neurotoxicity assessed by spatio-temporal modelling combined with artificial intelligence after brain radiotherapy, disponible sur www.health-data-hub.fr
3. Study of Neurological Complication After Radiotherapy for High Grade Glioblastoma www.irsn.fr/epibrainrad
4. Salivary dysfunction after radioiodine treatment www.irsn.fr/etude-start
Lors d'une radiothérapie, la tumeur est irradiée par des rayonnements ionisants. Ceux-ci peuvent affecter le tissus sains avoisinants. Des recherches et des expertises contribuent à limiter ces dégâts.
Un patient doit être traité par radiothérapie pour un cancer de la prostate. Tout au long du traitement, l'IRSN veille à réduire les risques pour ce patient.
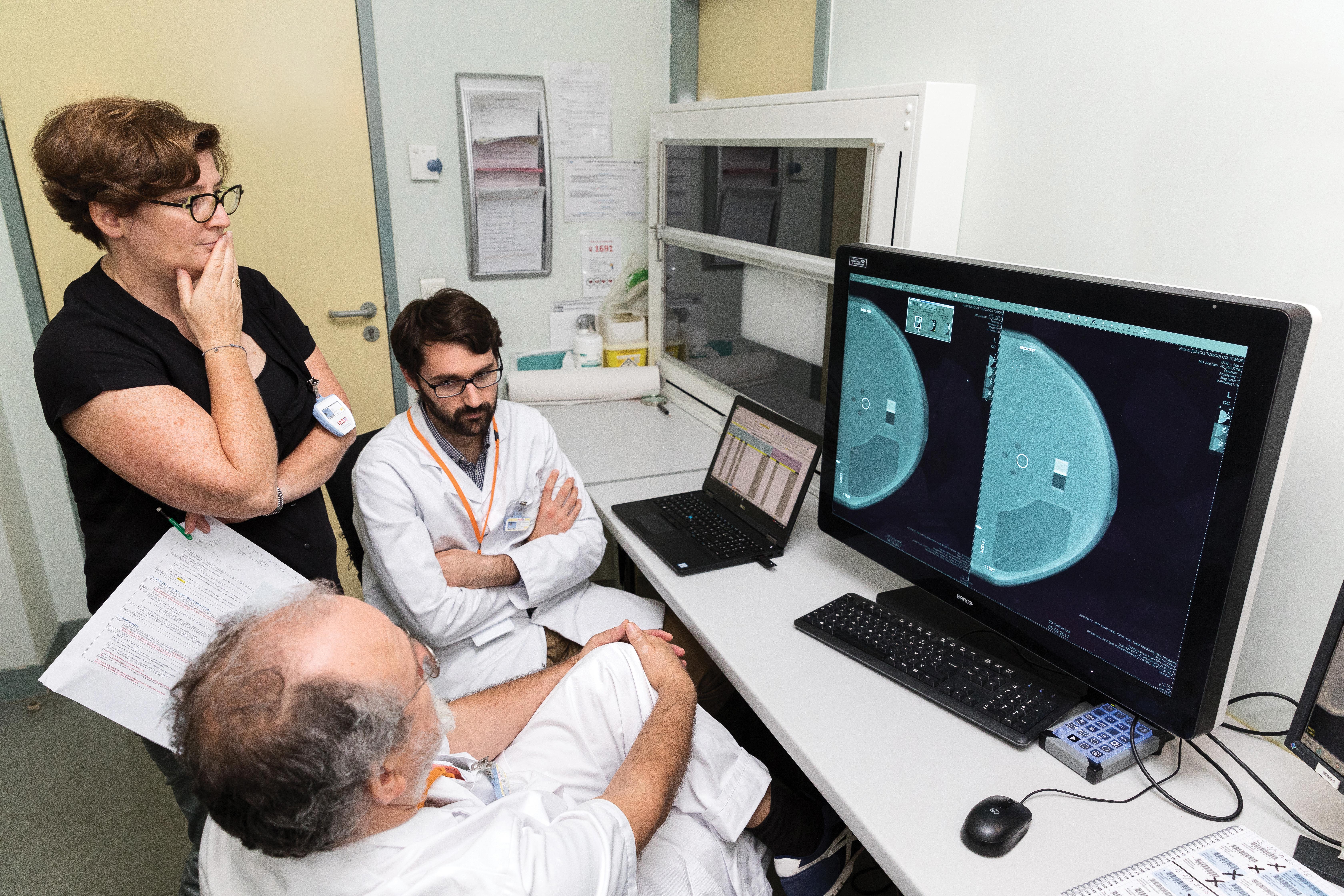
La tomosynthèse est de plus en plus utilisée pour l’imagerie du sein1. En 2021, elle ne dispose d’aucun niveau de référence diagnostique (NRD). Or ces derniers aident les praticiens à ajuster les doses délivrées lors des examens. Pour combler cette lacune, l’IRSN enquête entre mars et juillet 2021 auprès des professionnels. Avec des sociétés savantes*, l’Institut recueille les données de 3 009 patientes issues de 44 installations.
Dans ce type d’imagerie, plus l’épaisseur du sein compressé est importante, plus la dose délivrée est élevée. « Pour une bonne représentativité des différentes épaisseurs, nous préconisons de recueillir des doses pour au moins cinquante patientes par installation », expose Julie Sage, experte en radioprotection médicale. En appliquant ce principe au corpus de données collectées durant l’enquête, l’IRSN recommande de fixer le NRD pour une acquisition de tomosynthèse à 2,3 mGy. Il est déduit du 75e centile2 de la distribution des doses émises par ces 44 appareils.
En parallèle, une expertise est menée pour la mammographie numérique 2D directe, la plus utilisée pour le dépistage. Elle concerne 5 300 patientes et 77 appareils. Une nouvelle définition du NRD prend mieux en compte la diversité anatomique des femmes, sur le même principe de recueil que pour la tomosynthèse. L’IRSN recommande de fixer ce NRD à 1,7 mGy.
1. La tomosynthèse mammaire reconstitue différents plans du sein a diverses profondeurs (pseudo 3D) a partir d’images obtenues sous différentes projections.
2. 75 % des médianes des doses par installation sont inferieures a la valeur de NRD recommandée pour ce type d’examen.
* Société française de radiologie, Fédération nationale des médecins radiologues, Société d’imagerie de la femme, Société française de sénologie et de pathologie mammaire, Association française du personnel paramédical d’électroradiologie, Société française de physique médicale.
séances de radiothérapie sont effectuées en 2021 en faveur de 214 000 patients.
physiciens médicaux et ingénieurs travaillent à l’Unité d’expertise en radioprotection médicale (UEM).
sont suivis par des études épidémiologiques de l’IRSN pour mieux caractériser les effets secondaires de la radiothérapie pour des cancers du sein, de la thyroïde, du cerveau*.
* Études Baccarat, Early-Heart, Start, Radio-Aide et EpibrainRad.
Anticiper les effets secondaires des Nouvelles techniques de radiothérapie, Pour la science, 2020. www.irsn.fr/actu-pls3

Qu’elle ait besoin d’une imagerie diagnostique ou d’une radiothérapie, la femme enceinte peut être exposée aux rayonnements ionisants. Quelles procédures de radioprotection diminuent le risque pour l’enfant à naître ? Quelles expertises apporte l’Institut dans ce contexte ?
Article publié en septembre 2023